Основные определения, характеристика и область применения литейных сплавов.
Механические свойства литых заготовок.
В существующих ГОСТах регламентируется качество более 200 литейных сплавов.
Отливки из 400 литейных сплавов изготовляются по техническим условиям, принятым изготовителем и, естественно, потребителем.
Кроме того, практически из любого сплава (металла), даже нелитейного, можно изготовить отливку.
Поэтому ограничений по сплавам, а также по отливкам, которые принимают форму под действием силы тяжести, практически нет.
Основными критериями могут быть экономический фактор и возможность выполнения технических требований на предприятии.
Фасонные литые изделия используют во всех без исключения областях промышленности, строительства и быта.
В повседневной жизни нас повсеместно окружают отливки: металлические украшения, детали квартирных замков, сковородки, чугунки, ванны, краны, радиаторы, литые детали механизмов и машин.
В среднем на долю литых деталей приходится около 50% массы машин и механизмов, а их стоимость достигает 20...25% стоимости машин.
Сплавом называют вещество, образованное сплавлением двух или более металлов или металлов с неметаллами (железо с углеродом, алюминий с кремнием и т.п.).
В зависимости от метода получения заготовок сплавы подразделяют на литейные и деформированные.
В состав сплава входят: основа, легирующие добавки и примеси.
Основой сплава является металл, обычно один, определяющий его служебные свойства и стоимость.
Л е г и р у ю щ и м и называют элементы, которые вводятся в сплав специально для управления его служебными и технологическими свойствами.
П р и м е с я м и называют элементы, содержание которых незначительно и которые попали в сплав из руды, топлива, атмосферы, шлаков.
По воздействию на служебные характеристики сплава примеси подразделяются на вредные, т.е. снижающие свойства сплавов (например, S и Р во многих сплавах), и нейтральные, не оказывающие влияния на его свойства.
Отдельную группу составляют модификаторы — вещества, вводимые в малых количествах с целью управления главным образом размерами и формой зерна.
К основным критериям качества литого металла относятся механические свойства, показатели структуры, испытания износостойкости, коррозионной стойкости и т.п., заданные в технических требованиях.
Механические свойства определяются структурой и газоусадочной пористостью, которая практически всегда образуется в отливках.
На рис. 1. представлена зависимость соотношения временного сопротивления при растяжении плоских образцов стали 35Л, вырезанных из отливок и охватывающих все их сечения, и стандартных образцов, вырезанных из пробных брусков, от пористости рассматриваемого сечения отливки.
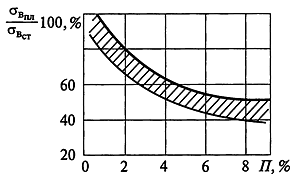
Рис. 1. Зависимость соотношения значений временного сопротивления плоских образцов, охватывающих все сечения стенки отливки, и стандартных образцов, вырезаемых из пробных брусков, от пористости П стенки стальных отливок
При пористости 6 % значение σвпл / σвст для всего сечения уменьшается на 50%, в том числе свойства металла поверхностного слоя снижаются на 20%, а осевой части — на 80 %.
Аналогичная зависимость была получена для металла с увеличением объемной доли неметаллических включений.
Слиток для последующей прокатки (обработки давлением) имеет такую же газоусадочную пористость и определенную долю (0,1...0,5 %) неметаллических включений.
В процессе прокатки (обработки давлением) металл уплотняется с заметным повышением механических свойств.
Поэтому для литейных сплавов при указании их марок в конце в обязательном порядке ставится буква «Л», свидетельствующая о том, что сплав литой, т.е. ему присущи отмеченные выше недостатки.
Однако в настоящее время литейное производство располагает технологиями изготовления практически плотных отливок, а также технологиями пропитки отливок и их газостатирования.
Сведения из теории плавления, кристаллизации и затвердевания металлов и сплавов.
Плавление, строение и свойства жидкого металла.
Плавление.
Для литейного производства необходим расплавленный жидкий металл, который должен принимать конфигурацию литейной формы с минимальными затратами энергии (в большинстве случаев должно быть достаточно силы тяжести).
При нормальных условиях и начальной температуре Тн металл находится в твердом состоянии, т. е. чтобы перевести его в жидкое состояние, металл необходимо нагреть до температуры плавления.
Процессы нагрева, плавления и перегрева до температуры заливки Тзал чистых металлов и эвтектических сплавов характеризуются изменением температуры металла (рис.2.) и его объема (V1 при температуре Тзал; V2, V3 при Ткр и Vо при Тн) (рис.3).
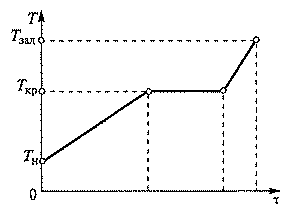
Рис. 2. Кривая нагрева чистого металла или эвтектического сплава
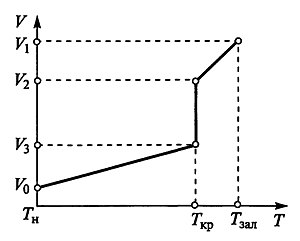
Рис. 3. Изменение объема чистого металла или эвтектического сплава при нагреве
Температура фазового перехода из твердого состояния в жидкое Tкр в течение некоторого времени сохраняется постоянной, при этом наблюдается скачкообразное увеличение объема и соответствующее уменьшение плотности.
Постоянство температуры свидетельствует о равенстве количества теплоты, подводимой к металлу, и количества теплоты, расходуемой на его плавление, т. е. сообщаемой металлу так называемой скрытой теплоты плавления.
Поэтому, несмотря на нагрев металла, температура его в этот период остается постоянной.
Явление скачкообразного увеличения объема при плавлении (оно составляет чаще всего 2...7%), а следовательно, и соответствующего ему уменьшения объема при затвердевании создает серьезные проблемы для технологов при производстве отливок, так как является причиной усадочных раковин и усадочной пористости.
Причиной увеличения объема металла при нагреве на атомном уровне является не только увеличение амплитуды колебательных движений атомов по мере повышения температуры, но и их отрыв от узлов обычного равновесного состояния при температуре плавления.
Строение и свойства жидкого металла.
Из известных состояний материальных веществ (твердое, жидкое, газообразное и плазменное) жидкое состояние можно рассматривать как промежуточное между твердым и газообразным.
Согласно современным представлениям жидкое состояние металла ближе к его твердому состоянию.
Установлено, что расплавы металлов на атомном уровне обладают некоторой структурой ближнего порядка, в них сохраняется закономерное расположение атомов, но только в пределах нескольких межатомных расстояний от центра данного атома (т.е. действует ближний порядок).
В отличие от жидкостей в твердом металле порядок в расположении частиц сохраняется на любом расстоянии от центра каждого атома (т.е. действует дальний порядок).
На рентгенограммах газа распределение плотности (интенсивности потемнения) в зависимости от расстояния у от центра данного атома практически одинаковое (непрерывный фон) (рис. 4, а).
В жидкости распределение плотности изменяется волнообразно с наличием пологих (размытых) максимумов, и по мере удаления от данного атома волны затухают (рис. 4, б).
В твердом металле положениям соседних атомов будут соответствовать четкие максимумы, или дискретные полосы (рис. 4, в).
Размытость максимумов на рентгенограммах жидкости связана с непрерывным изменением положения атомов.
При повышении температуры жидкости размытые максимумы уменьшаются.
При приближении к температурам кипения структура жидкостей приближается к хаотической, характерной для газообразного состояния (см. рис. 4, а).
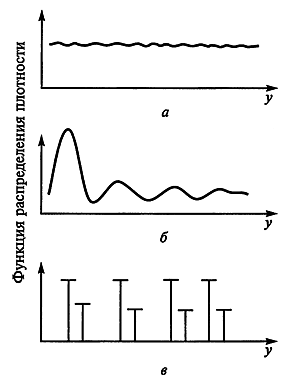
Рис. 4. Схемы рентгенографических спектров: а—газ; б—жидкость; в—твердый кристалл
Теплота плавления железа составляет 13,4 кДж/моль, а теплота испарения — 354 кДж/моль, т.е. энтальпийные величины различаются более чем на порядок.
Такая же картина наблюдается для других металлов.
В то же время изменение большинства свойств металлов (плотность, теплоемкость, электропроводность и др.) при изменении агрегатного состояния из твердого в жидкое, как уже отмечено выше, составляет 2...7 %.
Из этого можно сделать следующий вывод.
Если считать, что при испарении, т.е. при отрыве атомов, все связи между ними нарушаются и металлическая связь полностью исчезает, то при плавлении разрушается только 2...7 % этих связей, остальные же металлические связи продолжают действовать, т.е. колебательный процесс этих связей не претерпевает принципиальных изменений.
В работах Я. И. Френкеля и других ученых дана квазикристаллическая модель жидкости, в которой непрерывно возникают и разрушаются некоторые группировки с упорядоченным расположением атомов.
Строение металла в этих группировках соответствует строению твердого тела, хотя они и неустойчивы.
Устойчивость и продолжительность существования таких группировок повышается по мере охлаждения, т.е. приближения температуры жидкости к температуре плавления.
При некоторой определенной для каждого вещества температуре данные группировки должны приобрести полную устойчивость, став центрами кристаллов.
В научных работах такие группировки трактуются и называются по-разному: дозародыши (кристаллизации), флюктуации (отклонения от среднего), кластеры (гроздья) и т.п.
В многофазных сплавах в жидком состоянии можно ожидать существования группировок с повышенной концентрацией одного или нескольких компонентов, а также с наличием большой доли микроскопических и субмикроскопических частиц твердой фазы, в основном оксидов, нитридов, сульфидов, интерметаллидов, а в чугунах — графита.
По размерам такие частицы можно отнести к коллоидным, а реальный жидкий сплав во многих случаях является коллоидной (т.е. дисперсной) системой.
Выявлены также факты существования сравнительно устойчивых связей между структурой металла в жидком и твердом состояниях, или наследственности структуры, которая появляется и сохраняется при нескольких переплавах и кристаллизациях.
Описанные особенности строения расплавов имеют важное значение при рассмотрении вопросов плавки, кристаллизации и формирования структуры отливок.
В то же время интерес представляет поведение расплавов, являющихся коллоидными растворами, при течении по каналам литниковой системы и заполнении литейной формы.
Многочисленные исследования течения металлических жидкостей при температурах выше кристаллизационной в каналах с местными сопротивлениями (проведенные в том числе и в связи с проблемой использования жидкометаллических теплоносителей в ядерной энергетике) не показали разницы, в частности в потерях напора и распределении скоростей по сечению трубопроводов, по сравнению с течением нормальных ньютоновских жидкостей.
Гидравлические исследования течения металлов, выполненные с учетом специфических условий литейного производства, подтвердили вышеприведенный вывод.
На этом основании можно заключить, что для расчета процессов течения расплавов, в частности в литниковых системах, можно использовать положения гидромеханики, но при условии, что в процессе заливки не происходит затвердевание расплава.
Данных о гидравлических свойствах сплавов в температурном интервале между температурами ликвидуса и солидуса в настоящее время мало, однако достаточно, чтобы с уверенностью принять, что для рассмотрения вопросов течения в интервале затвердевания можно использовать реологические модели.
Для практиков очевидно, что без знания реологических характеристик затруднительно решить задачу об остановке потока в канале пробы при определении жидкотекучести, а также о заполнении литейной формы при реолитье (заливка частично закристаллизованного сплава).
Испарение.
Обычно под испарением понимают переход жидкости в парообразное состояние.
При некоторой температуре, существенно большей температуры плавления, начинается кипение жидкости, т.е. процесс ее интенсивного испарения не только со свободной поверхности, но и по всему объему жидкости.
В отношении литейных сплавов следует отметить, что жидкий металл имеет твердоподобную упорядоченную структуру только при небольших перегревах.
Если сравнить температуру плавления металлов tпл и температуру их кипения tкип, то для большинства металлов перегрев в 150 °С можно считать небольшим, составляющим порядка 10% от разности температур tкип— tпл (для Fe - tпл = 1539 °С, tкип = 2872 °С; для Al — tпл = 660 °С, tкип = 2520 °С), т.е. процессы испарения для такого интервала температур проявляются слабо.
Исключение составляют магний и цинк, которые используются как модификаторы или компоненты при производстве отливок из других сплавов с температурой плавления, превышающей температуру кипения этих двух металлов.
Магний используется при модифицировании чугуна с температурой заливки порядка 1400 °С (tкип = 1103 °С), а цинк является легирующим компонентом в латунях с температурой заливки 1050...1100 °С при tкип = 907 °С.
В названных производствах требуются специальные сберегающие технологии для уменьшения испарения, безвозвратных потерь и загрязнения атмосферы.
Особенно необходимо об этом заботиться при плавке в вакууме.
Кристаллизация. Зарождение и рост кристаллов.
У литейщиков принято разделять два понятия: затвердевание и кристаллизация.
Понятие з а т в е р д е в а н и я используется при определении объемов затвердевшего металла, толщин затвердевшей корки и времени затвердевания.
К р и с т а л л и з а ц и я используется при рассмотрении зарождения кристаллов, совместного их роста и формирования кристаллического строения отливки.
Образования кристаллов при переходе вещества из жидкого в твердое состояние принято называть «первичной кристаллизацией».
Изменение формы кристаллов в твердом состоянии называют «вторичной кристаллизацией».
Описательная теория кристаллизации металлов была создана Д.К. Черновым в 1870-е гг.
В начале ХХ в. Г. Тамман своими опытами показал, что для зарождения кристалла необходимо переохлаждение жидкого металла, что при отсутствии переохлаждения скорость кристаллизации и скорость возникновения центров кристаллизации равны нулю.
П е р е о х л а ж д е н и е м называется процесс охлаждения металла ниже температуры Ткр его равновесного перехода в другое фазовое состояние до температуры Т1.
Эту разность температур (Ткр—Т1) обозначают ΔТпереохл (рис. 5).
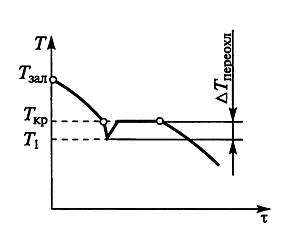
Рис. 5. Кривая охлаждения с переохлаждением
Для зарождения твердого кристалла необходима затрата энергии на образование поверхности раздела фаз — возникающей твердой и жидкой, поэтому в гомогенной (однородной) жидкости без переохлаждения зародыши возникнуть не могут (гомогенная кристаллизация).
Каждая фаза — жидкий металл 1, твердое тело 2 (рис. 6)— характеризуется индивидуальной зависимостью своей свободной энергии от температуры.
При температуре кристаллизации Tкр система фаз находится в динамическом равновесии, так как свободная энергия обеих фаз одинакова.
Устойчивей будет фаза, обладающая меньшей свободной энергией Гиббса, так как любая система стремится к равновесию, т.е. к состоянию, в котором значение ее свободной энергии в данных условиях минимально.
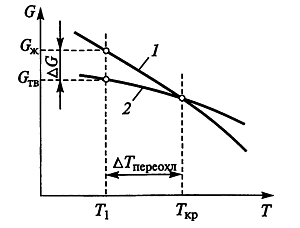
Рис. 6. Схема зависимости свободной энергии Гиббса G жидкой (1) и твердой (2) фаз от температуры
Охлаждение системы от равновесной температуры Tкр кристаллизации до температуры Т1 переводит ее в состояние, когда твердая фаза (зародыш) будет обладать меньшей свободной энергией и будет более устойчивой.
Разности температур ΔТпереохл соответствует разность свободных энергий жидкости (ж) и твердого (тв) тела:
Gж—Gтв = ΔG. (1)
Величина общей свободной энергии складывается из объемной и поверхностной:
ΔGv+ΔGs = ΔG. (2)
Если предположить, что зародыши имеют форму шара с радиусом r, то объемную энергию, за счет которой происходит снижение (—) общей свободной энергии, можно выразить через объем шара, теплоту кристаллизации L и относительное переохлаждение ΔТпереохл/Ткр:
ΔGv = - [LΔTпереохл / Tкр] · 4/3 πr3. (3)
В то же время повышение энергии (+) происходит в результате образования шаровой поверхности раздела фаз:
ΔGs = σ4πr2. (4)
Графически равенство (4) отражено на рис. 7.
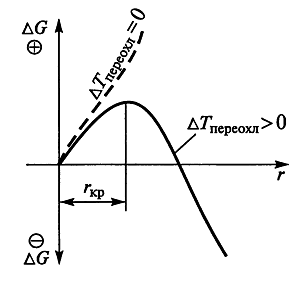
Рис. 7. Схема изменения свободной энергии системы в зависимости от радиуса сферического зародыша при различном переохлаждении
При малых значениях радиуса зародыша решающее значение будет иметь поверхностная часть энергии (+), при больших — объемная (—).
Между этими значениями, очевидно, существует критическое значение rкр, которому соответствует максимум энергии ΔG.
По мере увеличения радиуса rкр зародыша ΔG будет уменьшаться, а его устойчивость будет сохраняться, и зародыш сможет расти.
Размеры флюктуаций (группировок) с радиусом, меньшим rкр будут представлять собой неустойчивые дозародыши.
При переохлаждении ΔTпереохл = 0 радиус критического зародыша будет стремиться к бесконечности, и, следовательно, при температуре кристаллизации зародыш возникнуть не может.
При увеличении переохлаждения критический размер rкр зародыша будет уменьшаться, т.е. радиус устойчивого гомогенного зародыша связан с переохлаждением гиперболической зависимостью.
В реальных сплавах всегда присутствуют нерастворимые примеси, которые могут быть (и являются) твердыми подложками при кристаллизации.
Очевидно, что у зародыша, образовавшегося на таких примесях, меньшая по сравнению с теоретической поверхность (например, не полностью шар, а лишь сегмент шара на плоской подложке), и для его образования потребуется соответственно меньшее переохлаждение, чем для гомогенного зародыша такого же объема.
Образование зародышей на подложке называется г е т е р о г е н н ы м.
Изменения переохлаждения можно достичь изменением скорости охлаждения.
По данным профессора Б. Б. Гуляева при сравнительно больших скоростях охлаждения малоуглеродистой стали в тигле диаметром 10 мм достигалось значительное переохлаждение.
При увеличении диаметра тигля до 20 мм переохлаждение уменьшилось.
При дальнейшем увеличении диаметра тигля до 70 мм и соответствующем уменьшении скорости охлаждения термопара, установленная в центре, не фиксировала переохлаждение.
Диаметр тигля, в котором не отмечалось переохлаждения в центре, для алюминия был равен 100 мм, для сурьмы — 200 мм.
Поэтому разные металлы имеют разную склонность к переохлаждению.
Для больших масс переохлаждение жидкого металла отмечается перед фронтом кристаллизации и составляет 0,1...0,01 °С.
На основании описанных, а также других данных можно заключить, что с увеличением скорости охлаждения (затвердевания) переохлаждение увеличивается и, как результат, уменьшается размер зерна в отливке.
Уменьшение поверхностного натяжения, а следовательно, и уменьшение размера зерна может быть осуществлено введением в расплав поверхностно-активных добавок (модификаторов).
Уменьшение размеров зерна при увеличении переохлаждения связано с тем, что от переохлаждения зависят два параметра, известные из теории кристаллизации: введенная Г. Тамманом в начале ХХ в. скорость зарождения центров кристаллизации n (число центров, появляющихся в единичном объеме за единицу времени) и линейная скорость роста кристаллов v.
Оба эти параметра имеют одинаковый характер зависимости от переохлаждения (рис. 8).
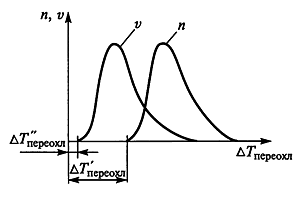
Рис. 8. Схемы зависимостей скорости n зарождения центров кристаллизации и линейной скорости v роста кристаллов от переохлаждения
Практически в обоих случаях реализуются только входящие ветви этих кривых.
Единственное различие заключается в следующем.
Величина ΔТ " определяет интервал переохлаждения, в котором скорость и зарождения кристаллов практически равна нулю и который называется интервалом метастабильности расплава.
Величина ΔТ " также определяет переохлаждение, но в данном интервале не происходит рост кристалла за счет перехода атомов из расплава в кристалл.
Следует отметить, что, как правило, ΔТ ' > ΔТ ".
Поэтому при размещении на одном графике кривые n и v будут смещены одна относительно другой, а их взаимное положение существенно влияет на окончательный размер зерна.
Например, при малых скоростях затвердевания и соответственно малых ΔТпереохл кристаллизация характеризуется малой скоростью и зарождения центров кристаллизации, но линейная скорость v роста при этом переохлаждении будет значительна, и в отливке образуется крупнозернистая структура.
С увеличением переохлаждения скорость n зарождения кристаллов будет увеличиваться, а скорость v роста кристаллов может не реализоваться, если иметь в виду один и тот же объем расплава.
Можно заключить, что скорость зарождения кристаллов n, скорость роста кристаллов v и критический размер зерна rкр зависят от переохлаждения и, следовательно, от скорости затвердевания или толщины стенки отливок, которая является одним из важных факторов, определяющих скорость затвердевания.
Кроме того, рассмотрение подробностей кристаллизации позволило расширить представление об известной зависимости (чем больше скорость охлаждения (затвердевания), тем мельче зерно отливки), установить наряду с тепловыми иные факторы управления размером зерна и объяснить многие экспериментальные сведения.
Типичной составляющей структуры отливки являются дендриты — древовидные разветвленные кристаллы.
Дендритное строение металла выявляется на макрошлифах.
Каждый дендрит образует отдельное макрозерно.
При травлении в зерне выявляются системы осей, располагающиеся под определенными углами одна к другой.
Границы между дендритами выявляются менее отчетливо, чем между округлыми зернами, которые также могут возникнуть в литой структуре.

Литература:
ISBN 5-7б95-127б-8
Литейные сплавы и плавка: Учебник для студ. высш. учеб. заведений / А. П. Трухов, А.И. Маляров. — М.: Издательский центр «Академия», 2004. — 336 с.
Рассмотрены литейные свойства наиболее распространенных промышленных сплавов.
|








