Кристаллизация металлов.
В кристаллах металла ионы располагаются правильными рядами и имеют определенную амплитуду колебаний.
При повышении температуры амплитуда увеличивается настолько, что правильность рядов нарушается и в жидком металле сохраняется только у ближайших соседей на протяжении нескольких параметров решетки.
При охлаждении жидкого металла наблюдается обратная картина.
С понижением температуры подвижность ионов падает и вблизи температуры плавления образуются скопления атомов, в которых они расположены, как в кристаллах, правильными рядами.
Такие скопления являются центрами кристаллизации (зародышами).
По достижению температуры затвердевания, вновь образуется кристаллическая решетка и металл переходит в твердое состояние.
Переход металла при определенной температуре из жидкого состояния в твердое называется кристаллизацией.
Энергетическое состояние любой системы характеризуется определенным запасом внутренней энергии, которая складывается из энергии движения молекул, атомов, электронов, энергии упругих искажений кристаллической решетки.
Та часть энергии, которая в изотермических условиях может быть превращена в работу называется свободной: E = U – TS,
где Е – свободная энергия, U – полная внутренняя энергия системы, T – температура, S – энтропия.
Чем больше свободная энергия системы, тем система менее устойчива.
Согласно второму закону термодинамики всякая система стремится к более устойчивому состоянию, т.е. к минимальному значению свободной энергии.
Любой самопроизвольно текущий процесс идет только в том случае, если новое состояние более устойчиво.
Например, шарик, поднятый на высоту Н, стремиться скатиться вниз по наклонной плоскости, уменьшив при этом свою свободную энергию (рис. 1).
Кристаллизация металлов также подчиняется этому закону: если меньшей свободной энергией обладает твердое тело, то идет процесс кристаллизации и наоборот, при меньшей свободной энергии жидкого состояния – плавление.
Зависимость изменения свободной энергии металла в жидком и твердом состояниях от температуры приведена на рис. 2.
С увеличением температуры величина свободной энергии как жидкой, так и твердой фаз уменьшаются.
Рис. 1. Изменение свободной энергии
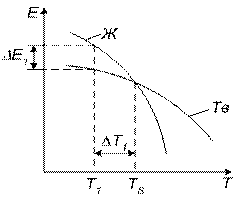
Рис. 2. Изменение свободной энергии (Е) жидкого (Ж) и твердого (Тв) металла в зависимости от температуры (Т °С)
При температуре Ts свободные энергии твердой и жидкой фаз равны, что дает возможность их одновременного существования.
Выше температуры Ts вещество находится в жидком состоянии, а ниже - в твердом состоянии.
Такая температура называется равновесной (или теоретической температурой кристаллизации).
Чтобы начался процесс кристаллизации необходима разность свободных энергий (∆Е1) жидкой и твердой фаз.
Это возможно при охлаждении вещества ниже температуры Ts.
В соответствии с этим температура Т1, соответствует температуре кристаллизации (или фактической температуре кристаллизации).
Разность по абсолютной величине между равновесной и температурой кристаллизации называется степенью переохлаждения: ∆Т = |Тs –Т1|.
Чем больше степень переохлаждения ΔТ, тем больше разность свободных энергий ΔЕ, тем интенсивнее будет идти процесс кристаллизации.
Для исследования процесса кристаллизации пользуются кривыми охлаждения.
Металл помещается в тигель из огнеупорного материала и нагревается до жидкого состояния.
Потом печь выключается, металл помещается в необходимую охлаждающую среду и записываются кривые охлаждения.
В качестве датчика температуры используются термопары.
Сначала происходит охлаждение жидкого металла.
Затем в нем появляются первые кристаллы, после чего снижение температуры на некоторое время приостанавливается, несмотря на то, что тигель продолжает терять тепло в окружающую среду.
Это тепло компенсируется скрытой теплотой кристаллизации.
На кривой охлаждения это соответствует горизонтальной площадке.
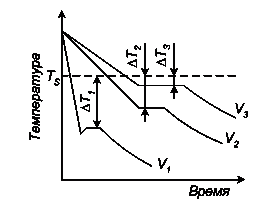
Рис. 3. Кривые охлаждения металла при различных степенях переохлаждения
Когда кристаллизация заканчивается, температура опять начинает снижаться, твердый металл остывает.
На рис. 3 приведены кривые охлаждения металла при различных степенях переохлаждения.
При незначительной степени переохлаждения (ΔТ3) скорость охлаждения (V3) сравнительно мала и кристаллизация протекает при температуре, близкой к равновесной.
При увеличении степени переохлаждения (кривые V2 и V1) скорости охлаждения увеличиваются.
Кристаллизация происходит при более низкой температуре и в течение более короткого времени.
Следует отметить, что чем чище металл, тем степень переохлаждения выше.
Впервые глубокие исследования процесса кристаллизации были проведены русским инженером – металлургом Д.К. Черновым в 1878 г. Он показал, что процесс кристаллизации складывается из двух этапов: образования центров и роста кристаллов из этих центров.
При снижении температуры жидкого металла до температуры кристаллизации группы атомов с упорядоченным расположением становятся устойчивыми и начинают обрастать новыми слоями, т.е. они становятся центрами кристаллизации.
Кристаллы свободно растут до тех пор, пока со всех сторон их окружает жидкий металл.
Когда кристаллов становится много, они мешают взаимному росту.
Поэтому кристаллы в металле имеют неправильную форму.
На рис. 4 показана схема роста зерен при кристаллизации.

Рис. 4. Соотношение роста зерен кристаллов и времени кристаллизации
За первую секунду на площади квадрата возникли пять зародышей.
К концу второй секунды эти зародыши выросли и одновременно возникли еще пять, уже на четвертой секунде кристаллы начинают мешать взаимному росту.
На седьмой секунде процесс кристаллизации заканчивается.
Как видно из схемы, по мере развития процесса в нем участвует все большее число кристаллов.
Поэтому в начальный момент кристаллизация идет более интенсивно.
После того, как половина жидкой фазы перейдет в твердую взаимное препятствие росту кристаллов замедляет процесс кристаллизации.
Этому же способствует и небольшое количество оставшегося жидкого металла.
Скорость процесса кристаллизации количественно характеризуется скоростью зарождения центров и скоростью роста кристаллов.
Число зарождающихся в единицу времени центров кристаллизации (Ч.Ц.) имеет размерность 1/мм3с (число центров, возникающих в 1 мм3 за секунду).
Скорость роста кристаллов (С.Р.) – это увеличение линейных размеров кристалла в единицу времени (м/ч).
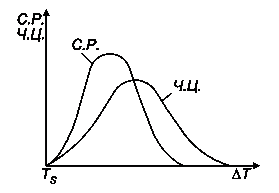
Рис. 5. Зависимость числа центров кристаллизации и скорости роста кристаллов от степени переохлаждения
Число центров кристаллизации и скорость роста кристаллов зависят от степени переохлаждения (рис. 5).
При равновесной температуре (ΔТ = 0) значения С.Р. и Ч.Ц. равны нулю.
Поэтому процесс кристаллизации идти не может.
При увеличении степени переохлаждения увеличивается разность свободных энергий твердой и жидкой фаз (рис. 3), что ведет к увеличению Ч.Ц. и С.Р.
Когда степень переохлаждения достигает больших значений (при низких температурах) подвижность атомов уменьшается, а это снижает Ч.Ц. и С.Р., т.е. способность системы к превращению уменьшается.
От соотношения величин С.Р. и Ч.Ц. при определенной степени переохлаждения зависят размеры кристаллов.
При большом значении С.Р. и малом Ч.Ц. (малая степень переохлаждения) образуются немногочисленные крупные кристаллы.
И, наоборот, при больших величинах ΔТ число центров велико, а скорость роста мала.
Поэтому образуется большое число мелких кристаллов.
При очень большой степени переохлаждения (при Ч.Ц. и С.Р. равным нулю) образуется аморфный металл.
Модифицирование металла.
Большую роль в количестве центров кристаллизации технических металлов и сплавов играют различные включения, попадающие при плавке или вводимые специально.
Такой метод является наиболее рациональным для регулирования размеров зерен, их формы, а, следовательно, и свойств.
Процесс искусственного регулирования размеров и форм зерен за счет введения дополнительных элементов называется модифицированием, а вводимые компоненты – модификаторами.
Наиболее часто в качестве модификаторов для стали используются алюминий, титан, ванадий; для чугунов – магний, церий.
По механизму воздействия модификаторы делятся на:
- вещества нерастворяющиеся в жидком металле - выступают в качестве дополнительных центров кристаллизации;
- вещества поверхностно-активные, которые растворяются в металле и, осаждаясь на растущих кристалла, препятствуют их росту.
Кристаллизация в формах и отливках идет в стороны противоположные отводу тепла, т. е. перпендикулярно стенкам и дну.
Вначале в этих направлениях образуется как бы ствол будущего кристалла, называемый осью первого порядка.
Одновременно на их ребрах происходит рост осей второго порядка, перпендикулярных первым.
Затем зарождаются и развиваются оси третьего порядка и т. д.
В итоге образуется древовидный кристалл, называемый дендритом...
|




